ベンゾジアゼピン,Z薬およびガバペンチノイド:依存,解毒および中止
先進国のほとんどで,ベンゾジアゼピン系薬剤やZ薬の使用は最長2-4週間までに制限されている1-3。しかし,英国では長期的に使用されることが依然として多く,300,000例の成人がベンゾジアゼピン系薬剤またはZ薬を12ヵ月超服用している4。NICEを含め,ほとんどのガイドラインで,ベンゾジアゼピン系薬剤またはZ薬の長期服用者には中止を勧めるよう推奨している。これは,ベンゾジアゼピン系薬剤またはZ薬に対する耐性(2-4週間後より発現しうる)により,長期的には不眠症および不安に対する有効性が失われるほか,依存が引き起こされて,離脱症状を防ぐためにのみ投与を継続することになる可能性があるためである(表3.27)5。
表3.27 ベンゾジアゼピン系薬剤の副作用
| 認知症状*11-13 | 精神障害と誤認する可能性のある反応14 |
|
|
|
|
|
|
*上記の障害の一部は服用中止後も持続する可能性がある。
ガバペンチノイド(GABAの類似体)もベンゾジアゼピン系薬剤とほぼ同じ作用機序を有し,同様の使用期間で中毒,身体的依存,離脱症状を引き起こしうる6-8。英国では計150万人にガバペンチノイドが処方されており9,処方数はこの10年間で7倍に増加している10。
これらのクラスの薬剤に依存している人々の大半は,薬剤を違法に入手しているのではなく,医師から処方されて服用している(いわゆる「医原性の依存症」)。
ベンゾジアゼピン系薬剤の長期使用は多数の問題と関連しており(表3.27),患者はそれらの問題を自覚しておらず,中止後に初めて認識するかもしれない16。Z薬の長期使用も同様のリスクに関連する17。ガバペンチノイドは自殺,意図しない過量服用,道路交通事故,頭部および身体の損傷18との関連が認められており,この薬剤に関しても長期使用の制限も賢明である可能性が示唆される。
離脱症状
ベンゾジアゼピン系薬剤,Z薬およびガバペンチノイドを中止することは困難な場合が多い(表3.28)。1件の研究で,患者の90%が中止時に離脱症状を経験し,半減期の長いベンゾジアゼピン系薬剤を服用していた患者の32%,半減期の短いベンゾジアゼピン系薬剤を服用していた患者の42%が,離脱症状のため服用を中止できないことが明らかにされた19。ジアゼパム等の長時間作用型より,ロラゼパム等の短時間作用型の薬剤の方が重度の離脱症状を生じやすい20, 21。これらの薬剤は長期使用では不安や不眠症に効果がないため,中止時に発現する症状は再発ではなく離脱症状である可能性が高い(ただし,症状は類似する場合もある)22。離脱症状の緩和後,精神状態は改善することが多い23。
表3.28 ベンゾジアゼピン離脱の影響24, 25
| 身体的症状 | 心理的症状 |
|
|
*通常,極めて急激な中止でのみ認められる。
これらの問題を回避もしくは軽減するためには,睡眠薬や抗不安薬としてベンゾジアゼピン系薬剤(およびZ薬)は,4週間以上処方すべきではない。可能な限り低用量での,(毎日ではなく)間欠的な使用とするのも賢明かもしれない。この点はガバペンチノイドにも当てはまると考えられる。
離脱症状の持続期間を検討した正式な試験は限られており,数週間持続するとの報告がいくつかあるが,特に長期使用の場合は1年超続く可能性もある20, 23。少数の患者では離脱症状が長引き,数年にわたって持続する場合があり,「急性離脱後症候群」と呼ばれることがある26。
ベンゾジアゼピン系薬剤の中止
患者の同意が得られればベンゾジアゼピン系薬剤を中止すべきである。漸減は困難な場合があり,患者の意思に反して強要すべきではない。クラスター無作為化試験は,対面での患者教育による介入の有効性を支持している27。患者に離脱症状に対する心構えをさせ,その過程を通じてサポートするために,継続的支援が必要な場合もある(例:心理療法や自助グループ)28。
減量の手順(漸減)
ベンゾジアゼピン系薬剤の用量を徐々に減らしていくと,離脱症状をより長期間に分散させる(かつ薬剤に対する神経順応が消失する時間を与える)ことで離脱症状の強さが抑えられる22。メタ解析では,徐々に減量(「漸減」)すると,ルーチンの臨床ケアと比較して中止率が改善することが確認されている29。ほとんどの研究で,10週間以上かけて段階的に中止する方法が,薬剤を使用しない状態を長期維持することに最も成功することが明らかにされているが30,患者の多くはそれよりはるかに長い期間(場合によっては数年間)を要するであろう。ベンゾジアゼピン系薬剤を突然中止すると致死的結果につながりうるため,必ず漸減が推奨される。
直接漸減するか,ジアゼパムに置換するか?
短時間作用型もしくは中時間作用型のベンゾジアゼピン系薬剤を使用している患者では,ベンゾジアゼピン系薬剤を直接漸減することができるが,1日1回を超える服用が必要かもしれない。
別の方法は,等価換算量のジアゼパム(半減期が長く,おそらく重度の離脱症状が誘発されにくい)への切り替えであるが20, 24,ジアゼパムに突然切り替えたことで離脱症状が報告された患者もいるため,段階的な切り替えが賢明であろう。コクラン・レビューでは,ジアゼパムへの切り替えは推奨も否定もされていない30。ベンゾジアゼピン系薬剤の「ジアゼパム等価換算量31」の概算を表3.29に示す。個体間の差により,離脱症状を抑制するために患者によってジアゼパムの用量を加減する必要があるかもしれない。
ベンゾジアゼピン系薬剤の半減期は薬剤によって大きく異なる。また,鎮静効果にも薬剤によって差があるため,正確な等価換算量を決めるのは難しい。したがって,表3.29はおおよその指針でしかない。肝機能障害がある患者では,ジアゼパムおよび他の長時間作用型の薬剤が中毒レベルまで蓄積する可能性があるため,特に注意が必要である。
表3.29 ベンゾジアゼピン系薬剤の「ジアゼパム等価換算量31」の概算
| クロルジアゼポキシド | 25mg |
| クロナゼパム | 0.5mg |
| ジアゼパム | 10mg |
| ロラゼパム | 1mg |
| ロルメタゼパム | 1-2mg |
| ニトラゼパム | 10mg |
| oxazepam | 20mg |
| temazepam | 20mg |
漸減パターン
ベンゾジアゼピン系薬剤の用量と,主な標的であるGABA-A受容体への作用との間には双曲線的相関があることから,以下の点が示唆される。
- 減量幅を固定すると(例:図3.6aでは12.5mgずつ),GABA-A受容体占有率の低下量が次第に大きくなる。
- これは,離脱症状が減量と非線形関係にある(例:ジアゼパムの1mgずつの減量は,20mgからであれば忍容可能だが,5mgからでは忍容不能である32)との臨床観察と一致する。
- ジアゼパムを50mgから5mg減量するとGABA-A受容体占有率は2.3パーセントポイント低下するが,5mgから5mg減量すると18.3パーセントポイント低下する。
ベンゾジアゼピン系薬剤を,主な標的への作用が同程度ずつ低減されるように減量するためには,用量を双曲線的に減らしていく必要がある(図3.6b)。
表3.6
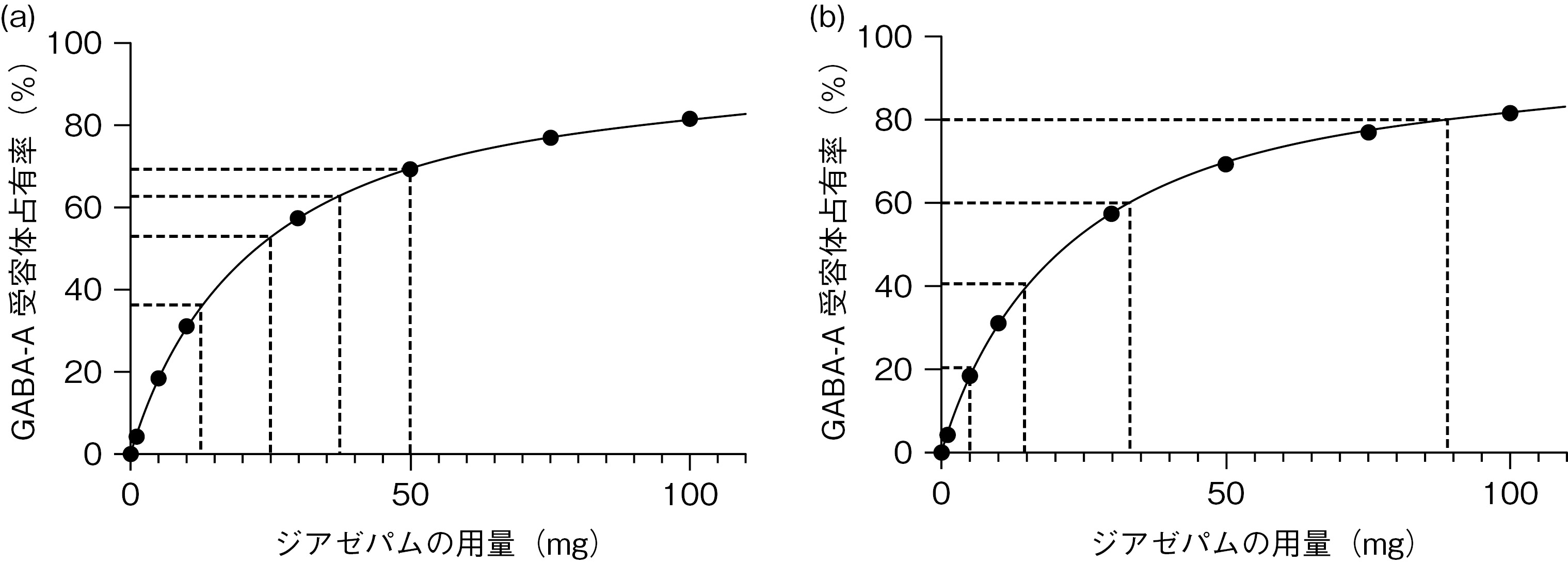
(a)線形的な減量ではGABA-A受容体占有率への作用の低下量が次第に大きくなる。
(b)GABA-A受容体への作用の低下量を一定に保つには,ジアゼパムの用量を双曲線的に減らしていく必要がある。最後の「ステップダウン」が大幅になりすぎるのを防ぐために,最後の数回はどれほど微量でなければならないかに注意されたい。出典:Brouillet et al. (199133)
- すなわち,減量幅が徐々に小さくなるようにしながら総投与量を減らしていくべきである。
- 実際には,直前の用量に対する比率(指数関数的パターン)に基づくと減量幅の算出が最も容易である。
- 2-4週毎に10%ずつの減量(直前の用量を基に算出。よって減量幅は徐々に減少)が忍容可能であると報告する患者が多いが,一部の長期使用者はさらに緩徐な減量を必要とするかもしれない。
- 完全中止までの最後の数回の用量はごく微量(多くの場合,ジアゼパム等価換算量1mgをはるかに下回る用量)とする必要があろう。
上記原則の実際の適用
漸減を開始する前に
- 種類を問わずベンゾジアゼピン系薬剤,Z薬,ガバペンチノイドの中止には,離脱症状のリスクが伴う(アルプラゾラム,ロラゼパムは高リスク)ことを,すべての患者に説明すべきである。
- ベンゾジアゼピン系薬剤を突然中止することは,けいれん発作を引き起こして死に至らしめる可能性があり,重度かつ長期持続する離脱症状を引き起こす可能性が最も高い方法であると考えられるため,突然中止しないよう患者に警告すべきである。
- ベンゾジアゼピン系薬剤の中止は不快な症状を引き起こしうるが,緩徐に慎重に漸減すれば,その過程は忍容可能と考えられる。過去に急速な漸減を経験した患者は安心させる必要がある。
- 数ヵ月,数年かけて漸減する患者がほとんどである。ただし,減量のペースは計画表を外部から無理にあてがうのではなく,個々の患者に忍容可能な範囲に応じて決定すべきである。
- 過去の減量の経験は,漸減期間中に生じるかもしれない症状を予測するのに役立つ場合がある。
- ベンゾジアゼピン系薬剤の漸減にあたって事前準備が必要となるかもしれない。例:仕事や家事の軽減または非薬物的な対処スキルの強化(受容,呼吸法,運動,趣味,日記,最悪の事態を考えすぎないこと,等)28, 34。
- 漸減期間中,不眠症がある患者にはメラトニンによる補助療法が有益となるかもしれず,パニック障害のある患者にはCBTが有益となるかもしれない24, 35, 36。用量の漸減に心理的介入(リラクゼーション,CBT)を併用すると,監視下での減量単独29や心理的介入単独37よりも成功しやすい。
- 患者と医師が多様な離脱症状(上記)を熟知しておくと,症状が発現したときに不必要な不安を軽減するのに有用かもしれない。離脱症状は薬剤が必要であることを意味するのではなく,漸減のペースを落とすべきであることを意味している。
用量漸減のプロセス
- 患者をおおまかにリスク層別化することができる。
- 低リスク患者(使用期間が6ヵ月未満,半減期の長いベンゾジアゼピン系薬剤,過去に重大な離脱症状を経験していない)では,25%の試験的減量を行ってもよい。
- 高リスク患者(使用期間が6ヵ月超,半減期の短いベンゾジアゼピン系薬剤,離脱症状の既往あり)では,5-10%の試験的減量を推奨する。
- 減量は直前の用量の比率(例:10%)に基づいて行うべきである。すなわち,減量幅が徐々に小さくなるようにしながら総投与量を減らしていくべきである。ほとんどの患者は,1ヵ月あたり直前の用量の約5-10%の減量ペースで進めていくことができる。
- 減量後は,2-4週間または症状が消失するまで,離脱症状をモニタリングすべきである。モニタリングには,症状の簡易な評価指標(例:10項目)を毎日用いるか,標準化されたベンゾジアゼピン離脱スケールを用いてもよい。
- さらなる減量は試験的減量の忍容性に照らして行うべきである。症状が忍容不能である場合は,増量,安定化の期間,より緩徐な減量が必要である。軽度の忍容可能な症状は,同じペースで減量を継続できることを意味している。
問題が発生した際の対応
- どの時点であれ重大な離脱症状が出現した場合は,現行の用量を維持して症状を消失させるか,忍容不能であれば,症状が忍容可能であった前回の用量に増量して,症状が消失するまでその用量を維持する。安定化した後は,減量幅をより小さくするか次の減量までの期間を延長する,あるいはその両方によって漸減をさらに緩徐に行う必要がある。
- 苦痛をもたらす離脱症状が認められる場合でも,ベンゾジアゼピン系薬剤を中止できないことを意味するわけではなく,これまでよりも減量幅を小さくして漸減の速度を落とす必要を示している(1ヵ月あたり直前の用量の5%未満の減量幅で漸減する必要のある患者もいる)。
- 用量がごく微量になると液剤が必要になる場合があり,ジアゼパムやロラゼパムなどの薬剤は液剤が利用できるため,これらの薬剤への切り替えは利便的である。他の選択肢として特殊な混合液などがある。多くの患者が,錠剤を分割して計量したり,錠剤を粉砕して溶液を作ったりしていると報告しているが,このような方法は推奨できない。
- 完全に薬剤を中止する前の数回の用量は,脳に対する作用が大きく低下することを避けるため,ごく微量とする必要がある。例えば,ジアゼパムを1ヵ月に10%ずつ減量した患者では,最終用量を0.25mgとする必要がある33。
減量スケジュール
ジアゼパムの減量のための簡易ガイド
- 2–4週間毎に5–10mg/日のペースで減量して50mg/日にする
- 2–4週間毎に2–5mg/日のペースで減量して20mg/日にする
- 2–4週間毎に1–2mg/日のペースで減量して10mg/日にする
- 2–4週間毎に0.5–1mg/日のペースで減量して5mg/日にする
- 2–4週間毎に0.25–0.5mg/日のペースで減量して2.5mg/日にする
- 2–4週間毎に0.1–0.25mg/日のペースで減量して中止する
他の薬剤クラスの漸減
Z薬やガバペンチノイドにも同じ原則が適用される。ガバペンチノイドは重度の離脱症状を引き起こす可能性があるが,個人間変動が大きい。Z薬は1日1回使用されるが,短期間または間欠的な使用の後でも,耐性および離脱症状が生じることが報告されている38, 39。中止するには,同様の指数関数的な計画に従った漸減(場合によってはジアゼパムへの段階的な置換)が必要となると考えられる。主な離脱症状は不眠および不安である。理想的には,睡眠を維持できるペースで漸減すべきである。
<編集協力者コメント>
日本においても行政主導で向精神薬多剤投与に対する規制が行われている。2022年4月時点で,保険医療機関が1回の処方において抗不安薬を3種類以上,睡眠薬を3種類以上,抗うつ薬を3種類以上,抗精神病薬を3種類以上,または抗不安薬と睡眠薬を合わせて4種類以上投与した場合には,向精神薬多剤投与の状況報告が必要で,診療報酬の減算がなされる。
(内田 貴仁)
参照文献
- BNF Online. British national formulary. 2020; https://www.medicinescomplete.com/mc/bnf/current .
- National Institute for Clinical Excellence. Guidance on the use of zaleplon, zolpidem and zopiclone for the short-term management of insomnia. Technical Appraisal [TA77]. 2004 (reviewed August 2010); https://www.nice.org.uk/guidance/ta77 .
- National Institute for Health and Clinical Excellence. Generalised anxiety disorder and panic disorder in adults: management. Clinical Guideline [CG113]. 2011 (last updated July 2019); https://www.nice.org.uk/guidance/cg113 .
- Davies J, et al. Long-term benzodiazepine and Z-drugs use in the UK: a survey of general practice. Br J Gen Pract 2017; 67:e609–e613.
- National Institute for Health and Care Excellence. Benzodiazepine and z-drug withdrawal. 2019; https://cks.nice.org.uk/topics/benzodiazepine-z-drug-withdrawal/?_escaped_fragment_=topicsummary .
- Schifano F, et al. An insight into Z-drug abuse and dependence: an examination of reports to the European Medicines Agency Database of Suspected Adverse Drug Reactions. Int J Neuropsychopharmacol 2019; 22:270–277.
- Evoy KE, et al. Abuse and misuse of pregabalin and gabapentin. Drugs 2017; 77:403–426.
- Public Health England. Advice for prescribers on the risk of the misuse of pregabalin and gabapentin. 2014; https://assets.publishing.service.gov.uk/government/uploads/system/uploads/attachment_data/file/385791/PHE-NHS_England_pregabalin_and_gabapentin_advice_Dec_2014.pdf .
- Marsden J, et al. Medicines associated with dependence or withdrawal: a mixed-methods public health review and national database study in England. Lancet Psychiatry 2019; 6:935–950.
- Gov.UK. Dependence and withdrawal associated with some prescribed medicines. An evidence review. 2020; https://www.gov.uk/government/publications/prescribed-medicines-review-report .
- Crowe SF, et al. The residual medium and long-term cognitive effects of benzodiazepine use: an updated meta-analysis. Arch Clin Neuropsychol 2018; 33:901–911.
- Brandt J, et al. Benzodiazepines and Z-drugs: an updated review of major adverse outcomes reported on in epidemiologic research. Drugs in R&D 2017; 17:493–507.
- Donnelly K, et al. Benzodiazepines, Z-drugs and the risk of hip fracture: a systematic review and meta-analysis. PLoS One 2017; 12:e0174730.
- Gutierrez MA, et al. Paradoxical reactions to benzodiazepines. Am J Nurs 2001; 101:34–39; quiz 39–40.
- Guina J, et al. Benzodiazepines I: upping the care on downers: the evidence of risks, benefits and alternatives. J Clin Med 2018; 7:17.
- Golombok S, et al. Cognitive impairment in long-term benzodiazepine users. Psychol Med 1988; 18:365–374.
- Finkle WD, et al. Risk of fractures requiring hospitalization after an initial prescription for zolpidem, alprazolam, lorazepam, or diazepam in older adults. J Am Geriatr Soc 2011; 59:1883–1890.
- Molero Y, et al. Associations between gabapentinoids and suicidal behaviour, unintentional overdoses, injuries, road traffic incidents, and violent crime: population based cohort study in Sweden. BMJ 2019; 365:l2147.
- Schweizer E, et al. Long-term therapeutic use of benzodiazepines. II. Effects of gradual taper. Arch Gen Psychiatry 1990; 47:908–915.
- Schweizer E, et al. Benzodiazepine dependence and withdrawal: a review of the syndrome and its clinical management. Acta Psychiatr Scand 1998; 98 Suppl 393:95–101.
- Uhlenhuth EH, et al. International study of expert judgment on therapeutic use of benzodiazepines and other psychotherapeutic medications: IV. Therapeutic dose dependence and abuse liability of benzodiazepines in the long-term treatment of anxiety disorders. J Clin Psychopharmacol 1999; 19:23S–29S.
- Ashton H. The diagnosis and management of benzodiazepine dependence. Curr Opin Psychiatry 2005; 18:249–255.
- Ashton H. Benzodiazepine withdrawal: outcome in 50 patients. Br J Addict 1987; 82:665–671.
- Soyka M. Treatment of benzodiazepine dependence. N Engl J Med 2017; 376:1147–1157.
- Petursson H. The benzodiazepine withdrawal syndrome. Addiction 1994; 89:1455–1459.
- Ashton H. Protracted Withdrawal From Benzodiazepines: The Post-Withdrawal Syndrome.Psychiatr Ann 1995; 1:174–179.
- Tannenbaum C, et al. Reduction of inappropriate benzodiazepine prescriptions among older adults through direct patient education: the empower cluster randomized trial. JAMA Int Med 2014; 174:890–898.
- Guy A, et al. Guidance for psychological therapists: enabling conversations with clients taking or withdrawing from prescribed psychiatric drugs. London: APPG for Prescribed Drug Dependence; 2019.
- Parr JM, et al. Effectiveness of current treatment approaches for benzodiazepine discontinuation: a meta-analysis. Addiction 2009; 104:13–24.
- Denis C, et al. Pharmacological interventions for benzodiazepine mono-dependence management in outpatient settings. Cochrane Database Syst Rev 2006; CD005194.
- Ashton H. Benzodiazepines: how they work & how to withdraw, the Ashton Manual. 2002; http://www.benzo.org.uk/manual/bzcha01.htm .
- Ashton H. Benzodiazepine dependence. Adv Syndrom Psychiatric Drugs 2004; 239–260
- Brouillet E, et al. In vivo bidirectional modulatory effect of benzodiazepine receptor ligands on GABAergic transmission evaluated by positron emission tomography in non-human primates. Brain Res 1991; 557:167–176.
- Inner Compass Initiative Inc. The withdrawal project. 2019; https://withdrawal.theinnercompass.org .
- Voshaar RCO, et al. Strategies for discontinuing long-term benzodiazepine use: meta-analysis. Br J Psychiatry 2006; 189:213–220.
- Fluyau D, et al. Challenges of the pharmacological management of benzodiazepine withdrawal, dependence, and discontinuation. Ther Adv Psychopharmacol 2018; 8:147–168.
- Gould RL, et al. Interventions for reducing benzodiazepine use in older people: meta-analysis of randomised controlled trials. Br J Psychiatry 2014; 204:98–107.
- Pollmann AS, et al. Deprescribing benzodiazepines and Z-drugs in community-dwelling adults: a scoping review. BMC Pharmacol & Toxicol 2015; 16:19.
- Kales A, et al. Rebound insomnia after only brief and intermittent use of rapidly eliminated benzodiazepines. Clin Pharmacol Ther 1991; 49:468–476.

