薬剤とアルコールの相互作用
薬剤とアルコールの相互作用は複雑である。本人関連要因,薬剤関連要因等,多くの要因を考慮しなければならない。様々なプロセスが同時に,または結果として生じる可能性があるため,転帰を正確に予測することは難しいかもしれない。
薬物動態学的相互作用1-4
アルコール(エタノール)は消化管から吸収され,体内水分中に分布する。女性や高齢者は分布容積が小さいため,ある一定量のアルコールを摂取した場合における血漿中アルコール濃度は若年男性に比べて高くなる。摂取したアルコールの約10%は初回通過効果を受け,アルコール脱水素酵素(ADH)で代謝される。ごく一部は胃でADHにより代謝され,残りは肝臓でADHおよびCYP2E1により代謝される。女性は男性に比べてADHによる代謝能力が低い。CYP2E1がアルコール代謝に果たす役割は機会飲酒者では小さいが,慢性大量飲酒者では重要な誘導性の代謝経路の1つである。CYP1A2,CYP3A4等その他多くのCYP酵素もいくらか代謝に関与している5, 6。
CYP2E1とADHはアルコールをアセトアルデヒドに変換する。アセトアルデヒドは「アンタビュース(ジスルフィラムの欧米での商品名)反応」として知られる不快な症状(例:紅潮,頭痛,悪心,倦怠感)の原因となる有害物質であり,また肝機能障害に関与する化合物でもある。アセトアルデヒドが向精神作用を及ぼす場合もある。エタノールは脳でCYP2E1によりアセトアルデヒドに代謝される7。体内酵素のカタラーゼも,脳やその他でアルコールをアセトアルデヒドに代謝することが知られている8。アセトアルデヒドはさらにアルデヒド脱水素酵素で代謝されて酢酸に変換された後,二酸化炭素と水に変換される。
アルコール代謝に関わる酵素には,いずれも遺伝子多型が存在する。例えば,北アジア出身者の多くはアルデヒド脱水素酵素による代謝能が低い9。酵素の機能はアルコールに反応して変化することがある。慢性的な飲酒はCYP2E1とCYP3A4を誘導する。その他の肝代謝酵素に対するアルコールの影響については,ほとんど研究が行われていない。
アルコールの代謝
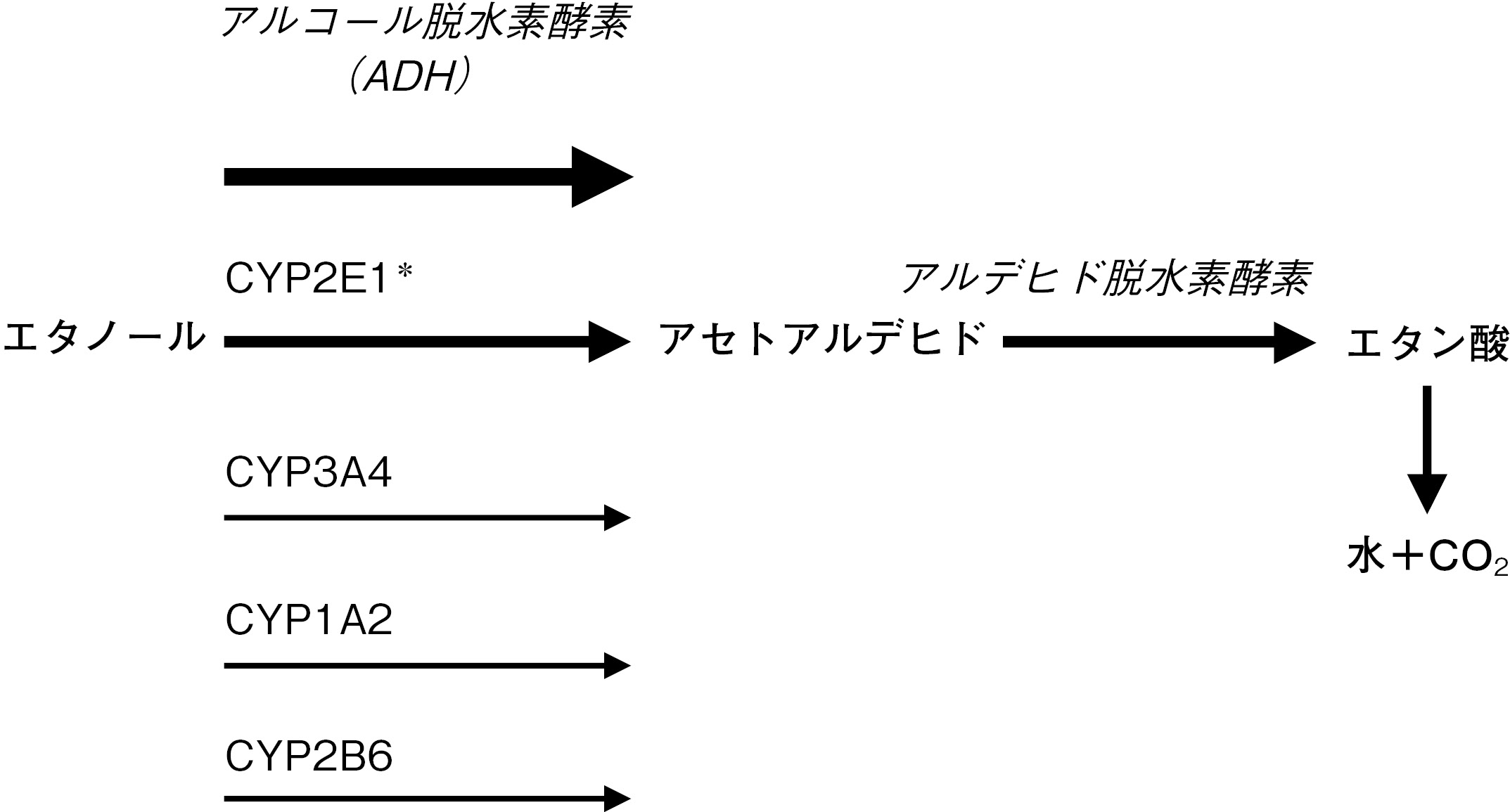
*機会飲酒者では重要ではないが,乱用者や血中アルコール濃度が高いときの重要な代謝経路となる。体内酵素のカタラーゼは広く分布しておりエタノールの代謝も行うことができるが,全体としてどの程度寄与しているかは明らかではない。
アルコール乱用者における相互作用は,飲酒している間または酩酊状態の際にみられる酵素作用部位における競合(薬剤の血漿中濃度上昇)と,しらふの際に優勢となる酵素誘導(薬剤の血漿中濃度低下8)の正反対の2つのプロセスが働いていると考えられるため,予測が困難である。慢性飲酒者,特に大量飲酒者では,酩酊期には処方薬の血清中濃度が毒性域に達し,しらふになると治療域以下に低下することがある。酩酊状態ではなくても,アルコールの同時摂取によりCYP3A4が競合的に阻害され,この酵素で代謝される薬剤の曝露量が増加するというエビデンスがいくらかある(表11.6)13。このため,身体疾患や精神疾患の治療の最適化が非常に難しい。
表11.5 アルコール脱水素酵素およびアルデヒド脱水素酵素を阻害する薬剤
| 酵素 | 阻害作用のある薬剤 | 起こりうる結果 |
| アルコール脱水素酵素 | アスピリン H2受容体拮抗薬 |
アルコール代謝が低下し,血漿中濃度上昇が長時間続く |
| アルデヒド脱水素酵素 |
クロルプロパミド ジスルフィラム griseofulvin イソニアジド 硝酸イソソルビド メトロニダゾール* nitrofurantoin スルファメトキサゾール tolbutamide |
アセトアルデヒド代謝能力が低下し,次のような「アンタビュース反応」が生じる:顔面紅潮,頭痛,頻脈,悪心および嘔吐,不整脈,低血圧 |
*メトロニダゾールがアルデヒド脱水素酵素に影響を及ぼすというエビデンスは,驚くほど弱い10-12。
表11.6 アルコールとCYP2E1やCYP3A4の基質を同時に摂取した場合
| 各酵素の基質(注:この一覧は全薬剤を網羅しているわけではない) | 患者が酩酊状態にある場合の作用 | 慢性飲酒者がしらふ状態にある場合の作用 | |
| CYP2E1 | paracetamol(アセトアミノフェン) イソニアジド フェノバルビタール ワルファリン ゾピクロン |
アルコールと薬剤が競合し,両者の代謝速度が低下する。血漿中濃度が上昇し,毒性が生じる可能性がある |
CYP2E1の活性が最大10倍に上昇する 薬剤の代謝が亢進し,治療が奏効しないおそれがある |
| CYP3A4 |
アルプラゾラム アリピプラゾール ベンゾジアゼピン系薬剤 カルバマゼピン クロザピン ドネペジル ガランタミン ハロペリドール メサドン ミルタザピン クエチアピン リスペリドン シルデナフィル 三環系抗うつ薬 バルプロ酸 ベンラファキシン Z系睡眠薬 |
アルコールと薬剤が競合し,両者の代謝速度が低下する。血漿中濃度が上昇し,毒性が生じる可能性がある | 薬物代謝が亢進し,治療が奏効しないおそれがある 酵素誘導は,アルコールの摂取を中止した後,数週間持続する可能性がある |
相互作用のなかには,ベラパミルの投与を受けている症例における血中アルコール濃度上昇,飲酒者におけるメチルフェニデート代謝低下等,原因が不明なものもある。
薬力学的相互作用2-4
アルコールはγ-アミノ酪酸(GABAA)受容体における抑制性神経伝達を増強し,N-メチル-D-アスパラギン酸(NMDA)型グルタミン酸受容体における興奮性神経伝達を抑制する(表11.7)。さらに,中脳辺縁系経路におけるドパミン放出を増大させ,セロトニン経路やオピオイド経路にも何らかの影響を及ぼすと考えられる。これらの作用により,アルコールは鎮静,健忘,運動失調を生じ,快感を増大させる(および/または,脆弱性を有する患者の精神病症状を悪化させる)と予想される。
表11.7 アルコールとの薬力学的相互作用
| アルコールの作用 | アルコールの作用を悪化させる薬剤 | 起こりうる結果 |
| 鎮静 |
鎮静作用のある他の薬剤 例:抗ヒスタミン薬 抗精神病薬 バクロフェン ベンゾジアゼピン系薬剤 lofexidine オピオイド チザニジン 三環系抗うつ薬 Z系睡眠薬 |
CNS抑制が増強され,不慮の事故の増加や,呼吸抑制,死亡にまで至る |
| 健忘 |
健忘作用のある他の薬剤 例:バルビツール酸系薬剤 ベンゾジアゼピン系薬剤 Z系睡眠薬 |
健忘作用が増加し,軽度の健忘から全健忘までみられうる。通常は前向性健忘で,アルコールの作用が出始めて以降の出来事の記憶を失う |
| 運動失調 |
ACE阻害薬 ß遮断薬 カルシウムチャネル拮抗薬 硝酸塩 アドレナリンα受容体拮抗作用をもつ薬剤 例:クロザピン リスペリドン 三環系抗うつ薬 |
不安定性の増大,転倒 |
アルコールは中脳辺縁系経路のドパミン放出を増大させることで,精神病症状を惹起ないしは悪化させる。抗精神病薬の作用に競合的に拮抗し,薬剤の効果を減弱させることもある(表11.8)。
表11.8 向精神薬:慢性飲酒者に対する選択
| 最も安全な薬剤 | 使用しないことが望ましい薬剤 | |
| 抗精神病薬 | スルピリドおよびamisulpride 持効性製剤が必要な場合はパリペリドン(鎮静作用がなく,腎から排泄される) |
クロルプロマジン,クロザピン等の鎮静作用の強い抗精神病薬 |
| 抗うつ薬 | SSRI─citalopram,セルトラリン CYP3A4を強力に阻害する薬剤(fluoxetine,パロキセチン)を慢性飲酒者に投与すると,アルコール代謝が低下することがある |
TCAはアルコールで代謝が障害され(酩酊時),血漿中濃度が上昇し,過量服薬の徴候・症状(著明な低血圧,けいれん発作,不整脈,昏睡)を起こすおそれがある 電解質障害により心臓に対する悪影響が増強する可能性がある TCAとアルコールを同時に摂取すると精神運動能力が著しく阻害される ミルタザピンは鎮静作用が強く出る場合が多い MAOIは著明な低血圧を起こすおそれがあり,チラミンを含有する飲料との相互作用により,高血圧クリーゼを起こす可能性もある |
| 気分安定薬 | バルプロ酸 カルバマゼピン 注:アルコール酩酊時には血漿中濃度が上昇し,忍容性不良となる可能性がある |
リチウムは治療域が狭く,アルコールに関連する脱水と電解質障害により,リチウムの毒性が発現するおそれがある |
注:慢性的なアルコール乱用者では肝不全や肝機能低下の可能性に注意する。Chapter 8の肝機能障害の項を参照のこと。
推奨されている薬剤であっても肝毒性のリスクがあることにも注意する(例:バルプロ酸)。
アルコール摂取に伴う脱水によって生じた電解質障害は,利尿薬等の電解質障害を引き起こす薬剤により,悪化するおそれがある。
インスリンまたは経口血糖降下薬を使用している糖尿病例では,大量飲酒によって低血糖症が生じることがあるので注意する。メトホルミン内服中の患者では,アルコール摂取によって乳酸アシドーシスのリスクが理論上高まる。アルコールは血圧を上昇させる可能性もある。
慢性飲酒者では,アスピリンおよび非ステロイド性抗炎症薬(NSAIDs)の胃腸刺激作用が特に発現しやすい。
注:薬物動態学的相互作用が存在すると,薬力学的相互作用がより顕著になる。例えば,慢性大量飲酒者がしらふのときは,酵素誘導によりジアゼパムの代謝が亢進し,不安が増加することがある(治療の失敗)。同じケースが酩酊時には,CYP3A4の代謝能力に対してジアゼパムとアルコールが競合するため,ジアゼパムの代謝が大幅に低下する。この結果,アルコールおよびジアゼパムの血漿中濃度が上昇する(毒性)。アルコールとジアゼパムにはいずれも鎮静作用があるため(GABAA受容体親和性による),意識消失や呼吸抑制が起こるおそれがある。
<編集協力者コメント>
日本人は,アルデヒド脱水素酵素による代謝能が低い遺伝子型を有することが多い。
(吉田 和生)
参照文献
- Zakhari S. Overview: how is alcohol metabolized by the body? Alcohol Research & Health: The Journal of the National Institute on Alcohol Abuse and Alcoholism 2006; 29:245–254.
- Tanaka E. Toxicological interactions involving psychiatric drugs and alcohol: an update. J Clin Pharm Ther 2003; 28:81–95.
- Wan Chih T. Alcohol-related drug interactions. Pharmacist’s Letter/Prescriber’s Letter 2008; 24:240106.
- Smith RG. An appraisal of potential drug interactions in cigarette smokers and alcohol drinkers. J Am Podiatr Med Assoc 2009; 99:81–88.
- Salmela KS, et al. Respective roles of human cytochrome P-4502E1, 1A2, and 3A4 in the hepatic microsomal ethanol oxidizing system. Alcohol Clin Exp Res 1998; 22:2125–2132.
- Hamitouche S, et al. Ethanol oxidation into acetaldehyde by 16 recombinant human cytochrome P450 isoforms: role of CYP2C isoforms in human liver microsomes. Toxicol Lett 2006; 167:221–230.
- Koster M, et al. Seizures during antidepressant treatment in psychiatric inpatients–results from the transnational pharmacovigilance project “Arzneimittelsicherheit in der Psychiatrie” (AMSP) 1993–2008. Psychopharmacology 2013; 230:191–201.
- Cederbaum AI. Alcohol metabolism. Clin Liver Dis 2012; 16:667–685.
- Wall TL, et al. Biology, genetics, and environment: underlying factors influencing alcohol metabolism. Alcohol Research: Current Reviews 2016; 38:59–68.
- Williams CS, et al. Do ethanol and metronidazole interact to produce a disulfiram-like reaction? Ann Pharmacother 2000; 34:255–257.
- Visapää JP, et al. Lack of disulfiram-like reaction with metronidazole and ethanol. Ann Pharmacother 2002; 36:971–974.
- Mergenhagen KA, et al. Fact versus fiction: a review of the evidence behind alcohol and antibiotic interactions. Antimicrob Agents Chemother 2020; 64:e02167–02119.
- Huang Z, et al. Influence of ethanol on the metabolism of alprazolam. Expert Opin Drug Metab Toxicol 2018; 14:551–559.

