抗精神病薬の高用量投与:処方とモニタリング
抗精神病薬の「高用量」投与は以下のいずれかによるものである。単剤での処方量が最大推奨用量を超えた場合,または複数の薬剤を使用しているときは,それぞれの薬剤の用量を最大推奨用量に対するパーセンテージに換算し,その合計が100%を超えた場合である1。実臨床では,抗精神病薬の多剤併用や抗精神病薬の頓用としての使用が高用量処方に強く関連する2, 3。
有効性
統合失調症に対して高用量の抗精神病薬を使用すれば,標準的な用量より高い有効性が得られる,という確実なエビデンスはない。精神症状を迅速に安定させたい場合,再発の予防,慢性的な攻撃性がある場合,急性期の精神病性エピソードの管理等を目的として使用する場合も同様である1。それにもかかわらず,英国では,入院患者の約1/4-1/3が高用量の投与を受けている2。一方,英国で2013年に行われた統合失調症に関する全国的な監査で,主に外来患者5,000人以上について処方の現状を調査したところ,全体で10%の患者が高用量の抗精神病薬を処方されていた4。
様々な抗精神病薬について用量反応関係を検討した結果,承認された用量以上に増量すると有効性が高まるというエビデンスはほとんどないことが明らかになった5, 6。リスペリドン4mg/日7,クエチアピン300mg/日8,オランザピン10mg9, 10等の低用量でも最適な効果が得られると考えられる。同様に,リスペリドンLAIは50mg/2週間の投与と比べて100mg/2週間の投与で利益があるわけではなく11,ziprasidoneも320mg/日が160mg/日より有効なわけではない12。クロザピン以外の現在市販されているすべての抗精神病薬は,主にシナプス後ドパミン受容体の拮抗薬(または部分作動薬)として作用する。一部の統合失調症では,ドパミン経路の機能不全が治療抵抗性の症状の原因とはいえないというエビデンスが増えており13-16,このような場合はドパミン遮断を強化しても意味があるかどうかは不確かである。同様に重要な点として,質量作用の法則により,いったん有効性の閾値に達すると,増量を行ってもドパミン受容体占有率の増加は次第に小さくなる17。
Doldら18は,無作為化比較試験(RCT)のメタ解析を実施し,抗精神病薬の標準用量での薬物療法に関する前方視的試験において奏効しないことが示されていた統合失調症患者を対象に,同じ抗精神病薬の標準用量の継続と増量を比較した。この場合には,増量により何らかの効果が得られるというエビデンスは認められなかった。なお,治療抵抗性統合失調症(TRS)と診断された患者を対象として,高用量と標準用量の有効性を比較したRCTがいくつかある1。高用量が有効であるとする試験もあるが19,大半の試験は古く,無作為化された患者数も少なく,現在の標準からすると不十分な研究デザインである。一部の試験では,クロルプロマジン10g/日を超える量に相当する用量を投与されていた。
統合失調症の初回エピソード患者を対象とした試験では,標準用量で奏効しない患者に対してオランザピンを30mg/日まで,リスペリドンを10mg/日まで増量しても,最終的な奏効率は4%(絶対値)しか改善せず,クロザピン等の抗精神病薬へ切り替えた方がはるかに奏効率は高かった20。高用量クエチアピン(最大1,400mg/日)の小規模非盲検試験(12例)では1/3の患者でやや有効であるという結果であり21,その他の大規模試験では高用量クエチアピンに利益はないことが示されている8, 22, 23。さらに別のRCTでは,高用量オランザピン(最大45mg/日)の有効性はTRSにおけるクロザピンと同程度であることが示唆されているが,症例数が少ないことを考慮すると,上記2剤が同等と結論付けるのは時期尚早であると考えられる24。TRSに対する標準用量を超えるオランザピンとクロザピンを比較した関連研究のシステマティック・レビューでは,オランザピンは,特に高用量ではTRSにおけるクロザピンの代替薬として検討できる可能性はあるが,有効性に関して最も堅固なエビデンスがあるのは依然としてクロザピンであると結論された25。
用量反応に関する最新の系統的解析26では,オランザピンとルラシドンはおそらく例外であるが,すべての抗精神病薬について,一定の用量を超えると用量反応曲線が平坦または水平になるという観察結果がほぼ支持された(オランザピンとルラシドンについては,承認範囲の上限にある用量が低用量よりやや有効性が高いというエビデンスがある10, 27)。この解析では,それを超えると追加の利益が得られにくくなるという用量は,上記の用量より若干高いことも示唆され,例えばリスペリドンは6.3mg/日,クエチアピンは482mg/日であった。しかし,重要な点として,いずれの薬剤についても,承認されている用量範囲を超える用量の使用を支持するエビデンスはなかった。
副作用
抗精神病薬の副作用の多くは用量に関連する。このような副作用としては,EPS,鎮静,起立性低血圧,抗コリン作用,QTc延長,冠動脈性心疾患による死亡等が挙げられる28-31。高用量の投与では,副作用の問題が明らかに大きくなる12, 23, 28, 32, 33。超高用量(クロルプロマジン等価換算値で平均2,253mg/日)から高用量(クロルプロマジン等価換算値で平均1,315mg/日)へ減量した結果,認知機能および陰性症状が改善したというエビデンスもいくつかある34。
推奨
- 実臨床では抗精神病薬の高用量投与は例外と考えるべきであり,クロザピンを含めた標準治療が奏効しない場合にのみ試みるべきである。
- 高用量の抗精神病薬を処方する場合は,患者にとってのリスクとベネフィットを継続的に考慮するために,可能であれば検証された評価尺度を用いて治療の標的となる症状,治療への反応,副作用等を評価し,記録することを標準的慣行とすべきである。身体のモニタリング(ECG等)を定期的に行うべきである。
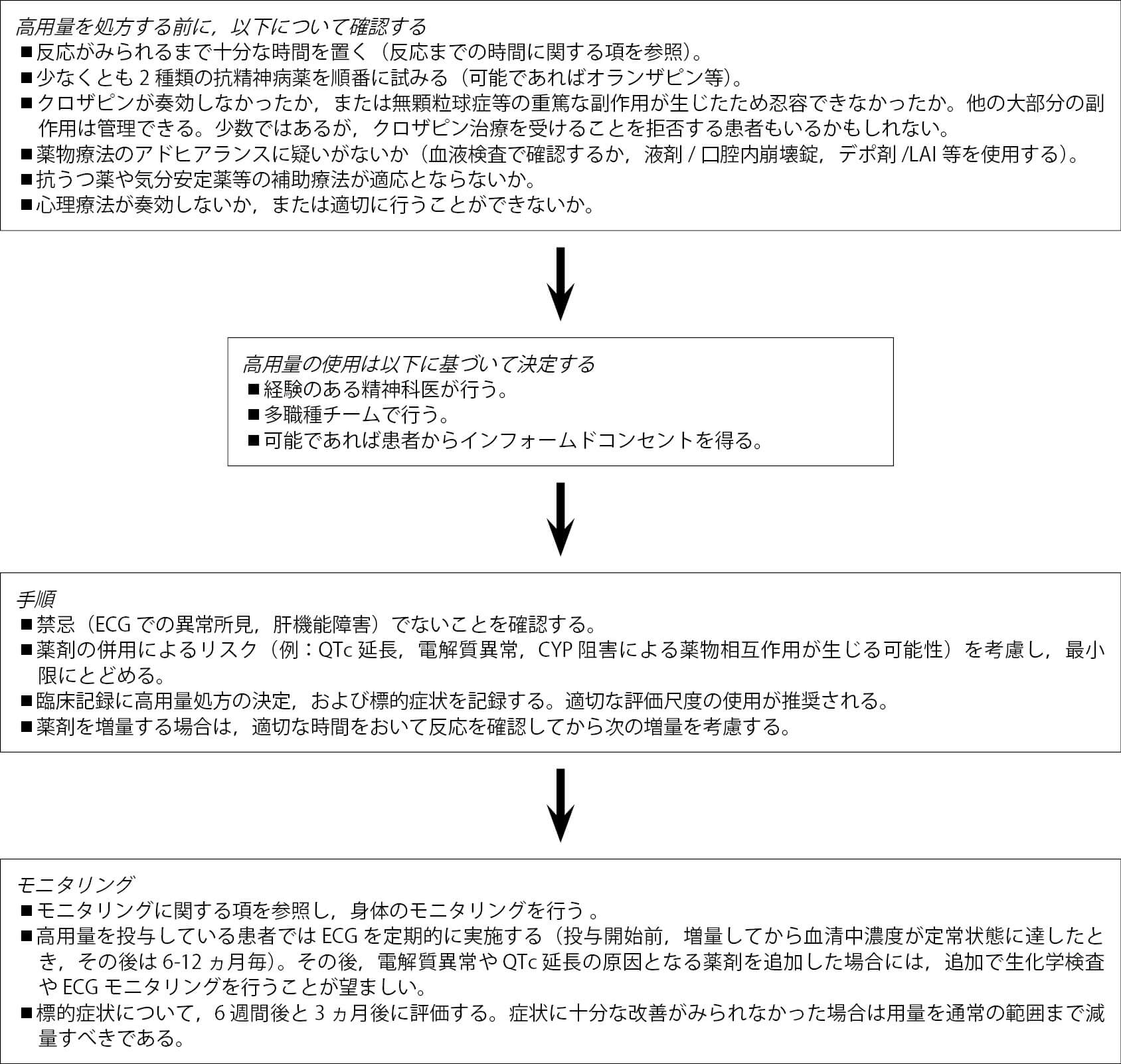
抗精神病薬の高用量投与
<編集協力者コメント>
- 抗精神病薬の大量投与は,本邦でも顕著である。
- 抗精神病薬の減量による改善は,副作用のみならず精神症状でも認めるとの報告もある。
- 低力価抗精神病薬の減量は,離脱症状の出現に注意を要する。
(谷 英明)
参照文献
- Royal College of Psychiatrists. Consensus statement on high-dose antipsychotic medication. College Report CR190 2014.
- Paton C, et al. High-dose and combination antipsychotic prescribing in acute adult wards in the UK: the challenges posed by p.r.n. prescribing. Br J Psychiatry 2008; 192:435–439.
- Roh D, et al. Antipsychotic polypharmacy and high-dose prescription in schizophrenia: a 5-year comparison. Aust N Z J Psychiatry 2014; 48:52–60.
- Patel MX, et al. Quality of prescribing for schizophrenia: evidence from a national audit in England and Wales. Eur Neuropsychopharmacol 2014; 24:499–509.
- Davis JM, et al. Dose response and dose equivalence of antipsychotics. J Clin Psychopharmacol 2004; 24:192–208.
- Gardner DM, et al. International consensus study of antipsychotic dosing. Am J Psychiatry 2010; 167:686–693.
- Ezewuzie N, et al. Establishing a dose-response relationship for oral risperidone in relapsed schizophrenia. J Psychopharm 2006; 20:86–90.
- Sparshatt A, et al. Quetiapine: dose-response relationship in schizophrenia. CNS Drugs 2008; 22:49–68.
- Kinon BJ, et al. Standard and higher dose of olanzapine in patients with schizophrenia or schizoaffective disorder: a randomized, double-blind, fixed-dose study. J Clin Psychopharmacol 2008; 28:392–400.
- Bishara D, et al. Olanzapine: a systematic review and meta-regression of the relationships between dose, plasma concentration, receptor occupancy, and response. J Clin Psychopharmacol 2013; 33:329–335.
- Meltzer HY, et al. A six month randomized controlled trial of long acting injectable risperidone 50 and 100 mg in treatment resistant schizophrenia. Schizophr Res 2014; 154:14–22.
- Goff DC, et al. High-dose oral ziprasidone versus conventional dosing in schizophrenia patients with residual symptoms: the ZEBRAS study. J Clin Psychopharmacol 2013; 33:485–490.
- Egerton A, et al. Dopamine and glutamate in antipsychotic-responsive compared with antipsychotic-nonresponsive psychosis: a multicenter positron emission tomography and magnetic resonance spectroscopy study (STRATA). Schizophr Bull 2020; 47:505–516.
- Kapur S, et al. Relationship between dopamine D2 occupancy, clinical response, and side effects: a double-blind PET study of first-episode schizophrenia. Am J Psychiatry 2000; 157:514–520.
- Demjaha A, et al. Dopamine synthesis capacity in patients with treatment-resistant schizophrenia. Am J Psychiatry 2012; 169:1203–1210.
- Gillespie AL, et al. Is treatment-resistant schizophrenia categorically distinct from treatment-responsive schizophrenia? A systematic review. BMC Psychiatry 2017; 17:12.
- Horowitz MA, et al. Tapering Antipsychotic Treatment. JAMA Psychiatry 2020; 78:125–126.
- Dold M, et al. Dose escalation of antipsychotic drugs in schizophrenia: a meta-analysis of randomized controlled trials. Schizophr Res 2015; 166:187–193.
- Aubree JC, et al. High and very high dosage antipsychotics: a critical review. J Clin Psychiatry 1980; 41:341–350.
- Agid O, et al. An algorithm-based approach to first-episode schizophrenia: response rates over 3 prospective antipsychotic trials with a retrospective data analysis. J Clin Psychiatry 2011; 72:1439–1444.
- Boggs DL, et al. Quetiapine at high doses for the treatment of refractory schizophrenia. Schizophr Res 2008; 101:347–348.
- Lindenmayer JP, et al. A randomized, double-blind, parallel-group, fixed-dose, clinical trial of quetiapine at 600 versus 1200 mg/d for patients with treatment-resistant schizophrenia or schizoaffective disorder. J Clin Psychopharmacol 2011; 31:160–168.
- Honer WG, et al. A randomized, double-blind, placebo-controlled study of the safety and tolerability of high-dose quetiapine in patients with persistent symptoms of schizophrenia or schizoaffective disorder. J Clin Psychiatry 2012; 73:13–20.
- Meltzer HY, et al. A randomized, double-blind comparison of clozapine and high-dose olanzapine in treatment-resistant patients with schizophrenia. J Clin Psychiatry 2008; 69:274–285.
- Souza JS, et al. Efficacy of olanzapine in comparison with clozapine for treatment-resistant schizophrenia: evidence from a systematic review and meta-analyses. CNS Spectr 2013; 18:82–89.
- Leucht S, et al. Dose-response meta-analysis of antipsychotic drugs for acute schizophrenia. Am J Psychiatry 2020; 177:342–353.
- Loebel A, et al. Lurasidone dose escalation in early nonresponding patients with schizophrenia: a randomized, placebo-controlled study. J Clin Psychiatry 2016; 77:1672–1680.
- Osborn DP, et al. Relative risk of cardiovascular and cancer mortality in people with severe mental illness from the United Kingdom’s General Practice Rsearch Database. Arch Gen Psychiatry 2007; 64:242–249.
- Ray WA, et al. Atypical antipsychotic drugs and the risk of sudden cardiac death. N Engl J Med 2009; 360:225–235.
- Barbui C, et al. Antipsychotic dose mediates the association between polypharmacy and corrected QT interval. PLoS One 2016; 11:e0148212.
- Weinmann S, et al. Influence of antipsychotics on mortality in schizophrenia: systematic review. Schizophr Res 2009; 113:1–11.
- Bollini P, et al. Antipsychotic drugs: is more worse? A meta-analysis of the published randomized control trials. Psychol Med 1994; 24:307–316.
- Baldessarini RJ, et al. Significance of neuroleptic dose and plasma level in the pharmacological treatment of psychoses. Arch Gen Psychiatry 1988; 45:79–90.
- Kawai N, et al. High-dose of multiple antipsychotics and cognitive function in schizophrenia: the effect of dose-reduction. Prog Neuropsychopharmacol Biol Psychiatry 2006; 30:1009–1014.

